没收到验证邮件?请确认邮箱是否正确或 重新发送邮件

#本文仅代表作者观点,未经作者许可,禁止转载,不代表IPRdaily立场#
来源:IPRdaily中文网(iprdaily.cn)
作者:田潇雨 上海星瀚律师师事务所
王洁敏 上海星瀚律师事务所
原标题:药品专利链接制度解读 | 品一品原研药企和仿制药企这碗水是如何被“端平”的
创新药物的研发具有高投入、高风险的特点。根据罗氏集团公布的数据显示,一个创新药物的研发要经过7000874小时的工作,6587次实验,423项研究,这些数据的完成大约需要12年的时间,以获得最终的研发药物。诚然,赋予创新药一定时期的垄断性权利是有效且唯一的激励机制。然而,药品因关乎人类的生命及身体健康而属于一类特殊的商品,如果给予原研药过长的技术垄断期限,将会严重影响社会公众对药品的可获得性。此时,药品专利链接制度承载着平衡原研药企与仿制药企之间利益冲突的使命而诞生。
一、 我国为什么需要专利链接制度?
所谓专利链接,是指仿制药上市审批与原研药品专利期满相“链接”,即仿制药注册申请应当考虑先前已上市药品的专利状况,从而避免可能的专利侵权。这一制度源于美国1984年通过的《药品价格竞争和专利期补偿法》(Hatch-Waxman Act)。
专利链接制度建立以前,国家药品监督管理局(以下简称“国家药监局”)在审批仿制药的注册申请时,往往不考虑药品专利权状况,仅对仿制药的安全性及有效性进行审核后即作出是否准予上市的决定。这样的审批程序,不仅会导致仿制药在原研药专利有效期内即可获批上市的尴尬局面,也将必然引发专利侵权纠纷。
对于大部分原研药企来说,专利保护期届满前的最后几年甚至几个月才是获得利益回报的关键节点,而几乎所有原研药企都难逃“专利悬崖”[1]的厄运。这种情况下,如果仿制药能够以更低廉的成本获得上市销售,并在原研药企本该享有垄断地位的市场中分得一杯羹,将会对原研药企构成极大的威胁。相反,对仿制药企来说,尽管获得了“强仿上市”,但其也时刻面临着被专利权人提起侵权诉讼以及司法禁令的风险。从这一角度来说,专利链接制度是原研药企与仿制药企共同的需求。
的确,我国药品市场发展的初期,中国主要以仿制药为主,相应的政策也能够清楚地反映出对仿制药企业的“偏爱”。而随着中国药企的经营模式由“以仿为主”逐步转为“仿创结合”,我国以美国《药品价格竞争和专利期补偿法》为范本,探索建立了“Bolar例外”原则、药品试验数据保护制度以及专利补偿期制度这三大板块。(见图一)
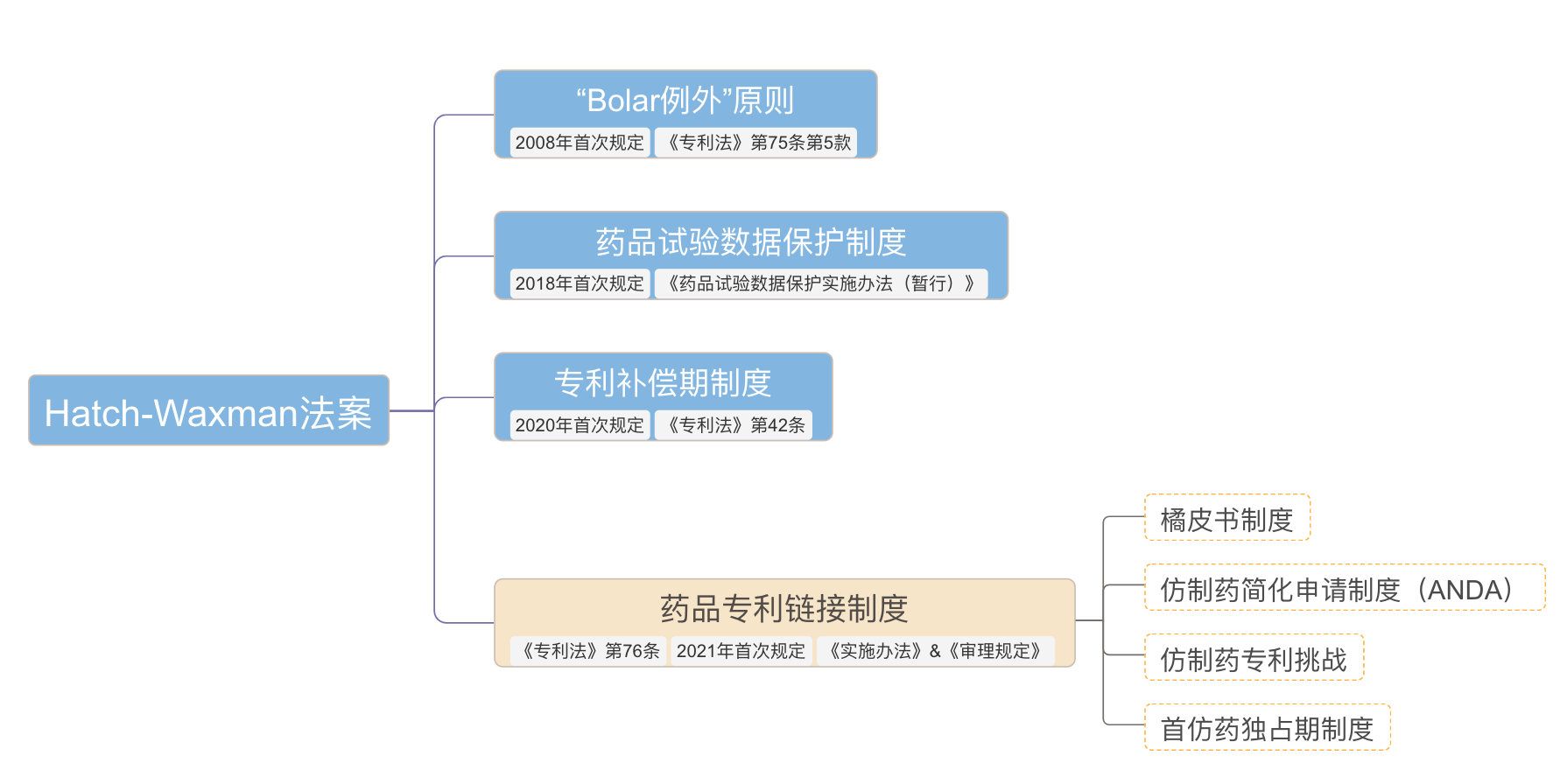
图一
2021年7月4日,国家药监局、国知局联合发布了《药品专利纠纷早期解决机制实施办法(实行)》(以下简称“《实施办法》”)。2021年7月5日,最高法发布施行《最高人民法院关于审理申请注册的药品相关的专利权纠纷民事案件适用法律若干问题的规定》(以下简称“《审理规定》”)、国知局发布《药品专利纠纷早期解决机制行政裁决办法》(以下简称“《行政裁决办法》”)。以上三份文件的颁布标志着我国平衡原研药企与仿制药企双方利益的最后一块制度版图已构建完成。
二、 专利链接制度为原研药企和仿制药企创设了哪些“权利义务”?
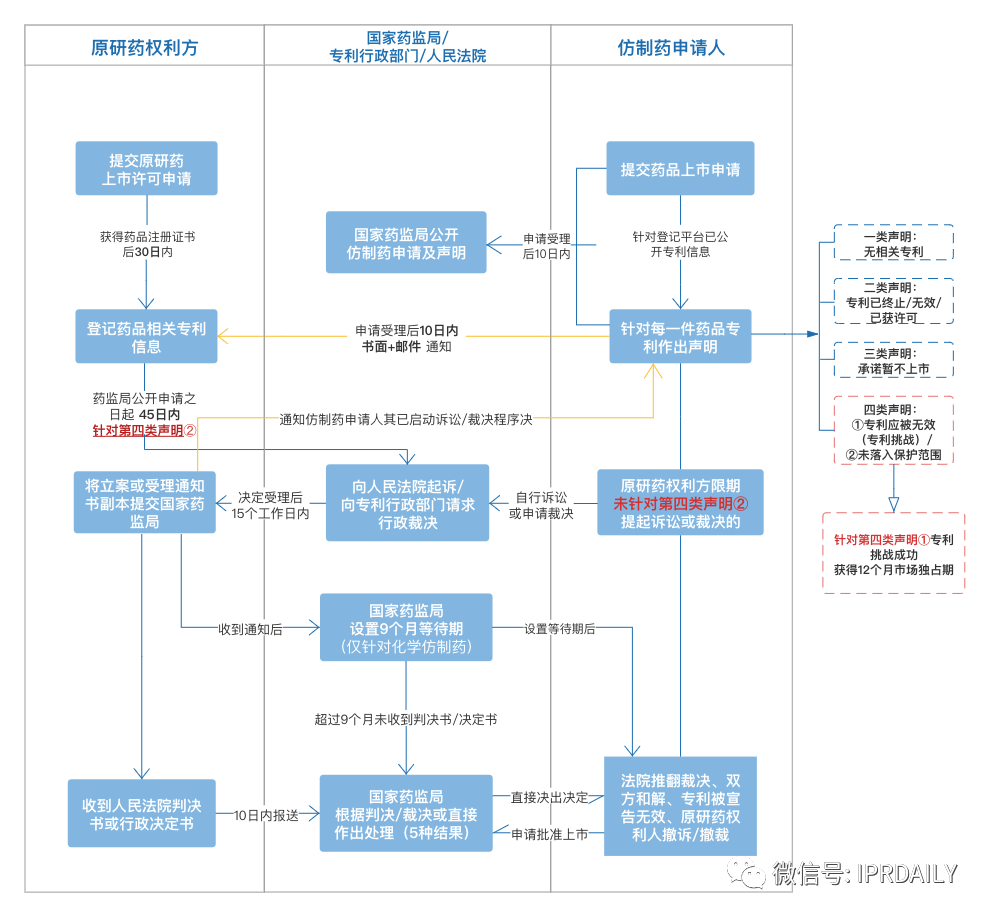
如前文所述,专利链接制度旨在通过设立药品注册与药品专利之间的衔接渠道,增进制药市场竞争状态并降低药品价格,从而为原研药企和仿制药企的并存发展建立相应的法律协调机制。为达到这一目的,前述三份文件为两方创设了基本对等的权利与义务(见图二),下文将逐一展开分析。
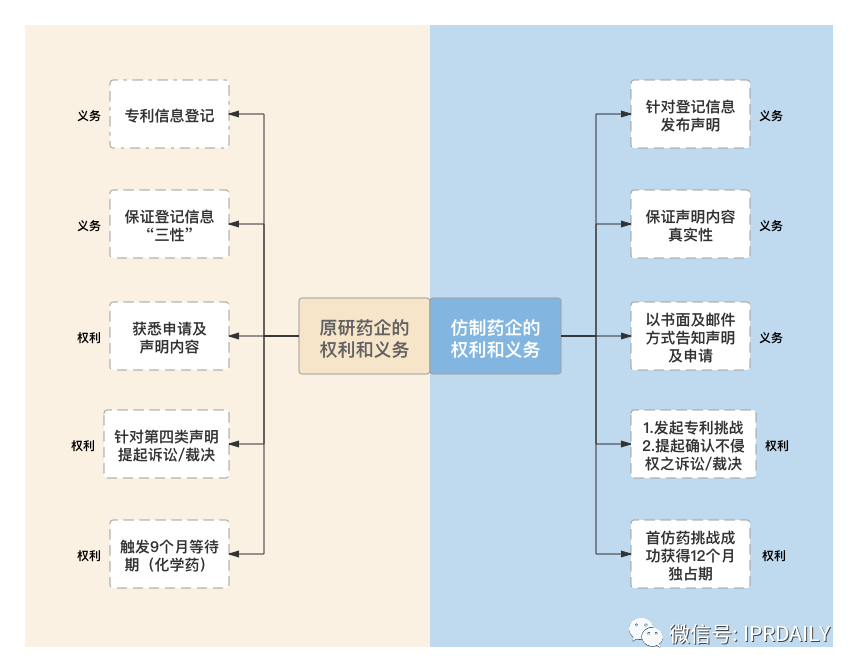
图二
(一) 原研药企的权利及义务
1、专利信息登记
《实施办法》第二条第二款明确了专利纠纷早期解决机制适用的前置程序,即专利链接制度仅解决已经在中国上市药品专利信息登记平台(以下简称“信息登记平台”)登记的专利产生的纠纷。同时,根据第四条之规定,登记主体应在获得药品注册证书后30日内自行完成登记。另外,以下三个方面值得注意:
(1) 登记主体
根据《实施办法》,提交上市药品登记信息的主体应为药品上市许可持有人。此处的药品上市许可持有人除包括药品的专利权人外,还包括专利被许可方。而在专利许可的情形下,仿制药申请人可以通过不同的许可方式判断药品上市许可持有人是否享有独立的诉权。
(2) 可否补登记
实践中,补登记包括以下两种情形下:第一,对于专利链接制度实施之前已经获得专利且获得上市批件的药品的追溯登记;第二,完成专利信息登记后又对新获得授权的专利的追加登记。对于第一种情形,通过对平台中已登记药品地检索,绝大多数药品获得注册证书与实际完成信息登记的期限间隔远大于规定的30日,由此对追溯登记给予了肯定的答复。而对于第二种情形,如果允许原研药权利方在完成专利信息登记后不断追加新的专利,仿制药申请人将很难攻破对方的“专利长青”战略,从而无限延长仿制药上市时间,这将不被专利链接制度所允许。因此,应当给予追加登记以否定的答复。
(3) 可登记的专利类型
根据《实施办法》政策解读所载明的内容,可登记的专利仅包括以下几类:
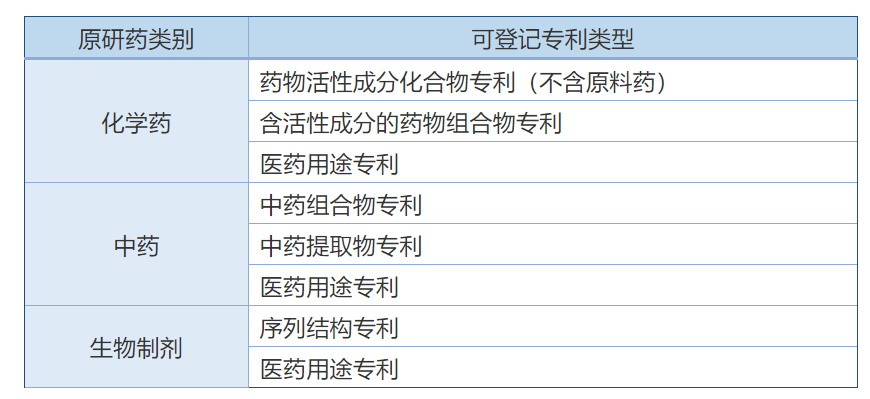
2、保证登记信息的“三性”
《实施办法》第四条第二款要求,药品上市许可持有人所登记的信息应当与药品相关专利信息、药品说明书所载明内容以及专利保护范围等内容相一致。对于仿制药申请人或者社会公众针对以上信息的真实性、准确性、完整性提出的异议,因及时核实并处理。同时,原研药权利方若存在不实登记或者不符合要求的登记行为,应承担相应的责任。可见,在细化性规定缺位的情况下,专利登记信息的“三性”主要依赖于上市许可持有人的自觉性。而专利信息登记作为专利链接制度的基础,其重要性不言而喻。因此,美国的公众异议制度或加拿大的登记审查制度就具有较强的参考价值。
3、及时获悉仿制药上市申请及声明
相较于《实施办法征求意见稿》,正式颁布的《实施办法》明确:仿制药上市申请被受理后的10个工作日内,原研药权利方应当能够通过以下两种方式获悉相应内容:①根据药品评审机构在信息登记平台公开的信息;②收到仿制药申请人的纸质和电子邮件通知。如此一来,原研药权利方可以根据仿制药的上市申请及声明类型提前制定应对策略,尤其是能够直接决定二者博弈胜负的第四类声明。
4、在异议期内针对第四类声明提起诉讼或裁决
此处需要强调的是,仿制药申请人的第四类声明包含两类:原研药专利应被宣告无效和仿制药未落入专利保护范围。而原研药权利方仅能够对后者提起诉讼或裁决。
面对两种不同的异议途径,原研药权利方应作何选择?综合《实施办法》、《审理规定》和《行政裁决办法》的具体规定,若选择向国务院专利行政部门提起行政裁决,仍可再向北京知产法院起诉。但若法院已受理立案,专利行政部门将不予受理。据此,原研药权利方在选择时可综合考虑两种途径的终局性、审限及其他相关因素。需要注意的是,根据《审理规定》第十条,如果权利方选择提起诉讼的,符合条件时可向人民法院申请行为保全,以禁止仿制药企的生产、销售及其他行为。
确定好异议方式后,权利方应在仿制药上市许可申请公开之日起45日内尽快启动程序,否则将丧失主动权。
5、原研药权利方诉讼或裁决行为将触发国家药监局9个月的等待期
根据《实施办法》第十条的规定,国家药监局在收到法院或专利行政部门的受理通知书后,将自动为仿制药的注册申请设置9个月的等待期,其中:
(1) 仅原研药权利方可触发9个月的等待期;
(2) 仅化学药仿制药可设置等待期;
(3) 等待期只可设置一次,自法院立案或行政部门受理之日起算;
(4) 等待期内国家药监局仅停止行政审批而不停止技术审评。
原研药权利方或仿制药申请人应于收到判决书或决定书10个工作日内将相应文书报送至国家药监局,对通过技术审评的化学仿制药申请,药监局将结合判决或决定作出以下处理:
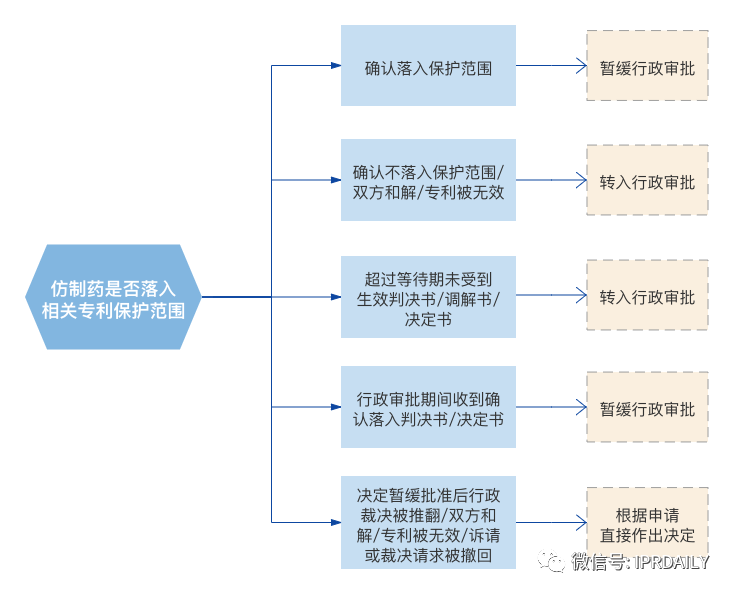
(二) 仿制药企的权利及义务
1、针对信息登记平台载明的信息作出声明
《实施办法》第六条向仿制药申请人提出了“在提交药品上市许可申请时一并提交声明”的要求。同时,专利声明应针对相关药品的每一件专利分别作出。具体来看,不同类型的声明及审批结果如下:
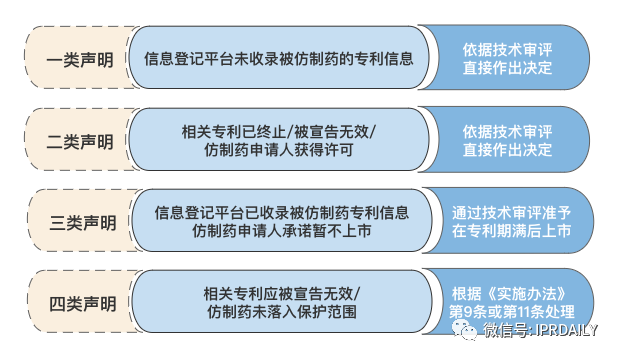
对于上述四类声明,仿制药申请人应在全面检索被仿制药的相关专利状况并结合仿制药预估的开发及上市销售时间后再作出。
2、保证声明内容的真实性
《实施办法》第六条同样为仿制药申请人提出了自觉保证相关声明真实性、准确性的要求。需要强调的是,若申请人提出未落入相关专利保护范围的声明,则需要提交仿制药的技术方案与被仿制药品专利权利要求的相关技术对比资料。并且,一旦任何一方启动诉讼程序,上述资料也将作为相应诉讼或答辩材料。
3、以书面及邮件方式告知原研药权利方相应申请及声明
如前文所述,仿制药企在提交上市申请后应通过书面+邮件的方式履行告知义务。设置这一义务的主要原因在于能够让原研药权利方第一时间获悉仿制药的存在并采取措施,避免原研药企花费大量的时间和精力监控仿制药的上市。
4、发起专利挑战或主动提起确认不侵权之诉讼/裁决
(1) 启动专利无效宣告程序,发起专利挑战。
首先,需要明确的是仅化学仿制药可以发起专利挑战。其次,基于专利无效宣告程序的一般规则,专利挑战成功的时间节点应以专利复审委员会审查决定作出的时间为准还是以权利人启动司法程序后的裁判结果的生效时间为准?尽管上述三份文件对此问题均未予以明确,但本文认为前者的时间似乎更符合专利链接制度的立法宗旨,即在仿制药上市前快速解决专利纠纷。否则,专利权人一旦启动司法救济程序,少则也需要再等待9个月的审限。
(2) 原研药权利方限期未行动,仿制药申请人主动提起确之诉/裁。
根据《实施办法》第八条第二款的规定,原研药权利方于申请公开之日起45日内未采取行动的,仿制药申请人可自行向北京知产法院或国务院专利行政部门提起仿制药未落入专利保护范围的确认判决。但通常情况下,45日期限届满,原研药权利方仍未提起诉讼或裁决的,国家药监局将直接开始行政审批程序,仿制药申请人似乎没有必要再花费额外的成本进行诉讼或裁决。
除此之外,《审理规定》第七条赋予仿制药申请人在提起诉讼时扩大诉请范围的权利,即仿制药申请人可主张已上市药品的专利属于现有技术或仿制药申请人享有先用权,并请求法院综合审查后再作出相应的确认判决。
5、首个挑战专利成功的化学仿制药将获得12个月的市场独占期
与原研药权利方触发9个月的等待期相类似,首仿药挑战成功后,也将获得12个月独占期限。在此期限内,仿制药不仅可以与原研药共同分割药品市场,还可以阻碍国家药监局批准同品种仿制药上市。尽管专利挑战难度不小,但是对于仿制药企业能够尽快在激烈的市场竞争中抢占一席之地的激励性同样也不小。
三、结语
总体而言,专利链接制度的核心价值在于鼓励当事人双方将专利纠纷提前至药品上市阶段,避免仿制药上市之后因专利权属纠纷而影响双方的销售盈利。除了制度指引和支持,专利链接制度也为我国的药品企业带来了新的机遇与挑战。尽管相应制度的建立无法停止原研药企与仿制药企之间的博弈,但只有在保证双方竞争地位对等的前提下,二者的博弈才能激发出更有价值的创新。
注释:
[1] “专利悬崖”是对药品专利保护期届满带来的专利药品销售和利润的大幅下降的形象比喻,将专利保护期届满时的界限形象比喻为悬崖。
来源:IPRdaily中文网(iprdaily.cn)
作者:田潇雨 上海星瀚律师师事务所
王洁敏 上海星瀚律师事务所
编辑:IPRdaily王颖 校对:IPRdaily纵横君
注:原文链接:品一品原研药企和仿制药企这碗水是如何被“端平”的(点击标题查看原文)
青年有为!寻找2021年“40位40岁以下企业知识产权精英”活动正式启动

「关于IPRdaily」
IPRdaily是具有全球影响力的知识产权媒体,致力于连接全球知识产权与科技创新人才。汇聚了来自于中国、美国、欧洲、俄罗斯、以色列、澳大利亚、新加坡、日本、韩国等15个国家和地区的高科技公司及成长型科技企业的管理者及科技研发或知识产权负责人,还有来自政府、律师及代理事务所、研发或服务机构的全球近100万用户(国内70余万+海外近30万),2019年全年全网页面浏览量已经突破过亿次传播。
(英文官网:iprdaily.com 中文官网:iprdaily.cn)
本文来自IPRdaily中文网(iprdaily.cn)并经IPRdaily.cn中文网编辑。转载此文章须经权利人同意,并附上出处与作者信息。文章不代表IPRdaily.cn立场,如若转载,请注明出处:“http://www.iprdaily.cn/

 共发表文章1634篇
共发表文章1634篇文章不错,犒劳下辛苦的作者吧
- 我也说两句
- 还可以输入140个字














