没收到验证邮件?请确认邮箱是否正确或 重新发送邮件

#本文由作者授权发布,未经作者许可,禁止转载,不代表IPRdaily立场#
来源:IPRdaily中文网(iprdaily.cn)
作者:王函 合伙人 王则周 律师 汇业律师事务所
原标题:补充数据规则变化对国内药企专利布局的影响——中美经贸协议下药品相关知识产权问题的思考(上)
近年来医药界争议比较大的一个问题:医药专利审查程序(包括实审、复审、无效)中的补充实验数据问题。2020年1月15日,中美双方正式签署的《中美经贸协议》中关于药品相关的知识产权中,提到了补充数据问题。本文主要对《中美经贸协议》中补充数据规则改变进行分析探讨。
引言
疫情期间,武汉病毒所申请专利引发热议,关于瑞德西韦药品相关专利得到公众关注。笔者在疫情期间写了一篇名为《武汉病毒所申请抗新冠病毒用途专利能否成功?》的文章,文章中提到:“武汉病毒所申请的瑞德西韦抗新冠病毒用途专利如果缺乏有效的对比实验数据来证明能带来预料不到的技术效果,很有可能因为不具备创造性而无法获得专利授权。”对此,有读者提问:如果武汉病毒所在专利申请后补充相关实验数据呢?这确实是一个很好的问题。我当时的回复是:武汉病毒所可以采取优先权的方式,即以在先申请为优先权基础,在申请日起一年内补充实验数据重新递交专利申请。随即,又有读者发问:如果在答复审查意见中补充实验数据是否可以?这就引发了近年来医药界争议比较大的一个问题:医药专利审查程序(包括实审、复审、无效)中的补充实验数据问题。
2020年1月15日,中美双方正式签署的《中美经贸协议》中关于药品相关的知识产权中,就提到了补充数据问题。本文主要对《中美经贸协议》中补充数据规则改变进行分析探讨。

一、《中美经贸协议》补充数据规则解读
《中美经贸协议》第1.10条 考虑补充数据:国内应允许药品专利申请人在专利审查程序、专利复审程序和司法程序中,依靠补充数据来满足可专利性的相关要求,包括对公开充分和创造性的要求。
本条款所涉的关于补充数据问题,是中美两国多年来一直在交涉的重要议题。早在2013年发布的《关于加强中美经济关系的联合情况说明》中,文本明确记载:“中方确认,中方的《专利审查指南》允许专利申请人在提交专利申请后提交额外的数据,《专利审查指南》适用《中华人民共和国立法法》第84条,确保药品发明获得专利保护。”本次中美第一阶段经贸协议再次将此项作为重要议题明文记载。那么,为何这一非常具体的技术和业务问题频频在两国高层磋商中亮相?这就要从药品专利的特点讲起。

二、药品专利的特点
首先,一般的发明比如机械发明,其技术效果一般可以通过技术方案本身即可获知,并不必要以实验证据来证明其效果。例如,增加或减少一个零部件,其对整个技术方案的影响,审查员可以根据该零部件的功能较为准确地推断。而药品发明则大为不同,药品的技术效果往往难以从药品的分子结构进行预测,必须借助于实验数据加以证实。有时候结构差异极小的物质,疗效却会大相径庭。极端的例子如二十世纪六十年代的“反应停”事件,该药品(沙利度胺,halidomide,N-(2, 6-二氧代-3-哌啶基)-邻苯二甲酰亚胺,俗称“反应停”)的R(+)构型具有对妊娠期妇女的镇静止吐作用,但与其分子结构完全相同仅一个手性原子构型不同的S(-)构型则导致欧洲1.2万婴儿致残,酿成药物史上最严重的不良反应事件。
其次,很多药物从最初的理论方向出发,并不是一款成功的药物,但是在临床过程中却发现了新的适应症,而被授予专利。如人们所熟知的万艾可,其最初研发的目的是为了治疗心绞痛,但是效果不佳,之后用于治疗勃起功能障碍异常成功。还有重磅药普瑞巴林,最初的研发目的是作为一种抑制神经传质的抑制剂,同样效果不佳,但是在临床过程中发现了其在缓解糖尿病周围神经病变和带状疱疹后神经痛的作用,成为目前世界上最畅销的镇痛药。
另外,衡量药品创造性的指标非常丰富,不单单有新的适应症。到针对适应症提供更有优势的治疗效果,例如更高的活性、更低的毒性、更合理的控释速度、更方便的给药途径等都可被视为具有创造性。甚至药品的储存稳定性、易加工性等特点也被视为药品专利应予考虑和接受的技术效果。
综上,药品专利的实验数据呈现出了与其他技术领域不同的特点。药品专利涉及化学、生物医药领域,属于实验学科,与其它技术领域相比存在明显区别,其撰写也存在特殊之处。化学、生物医药发明是否能够实施,往往难以预测,必须借助于实验结果加以证实才能确认。
三、美国与中国的补充数据规则之比较
美国原研药的研发能力强,因此对待药品专利的补充数据比较宽容。美国专利法对于说明书的书面描述的检验标准,其要求确定附加材料是否在原始申请中公开,确保发明人不能通过把后来的技术改进加入到在先提交的申请中而不适当地扩大其专利范围。但是实务中仅限于限制补充技术方案本身,而非拒绝提供用于证明效果的实验数据。根据美国专利权纠纷的判例来看,美国的法院认为,并无法律规定,在专利申请提出之前发明的属性或效果应完全知晓,或者专利申请中应包含发明研究的所有内容,为应对诉讼而在专利授权之后得到的证明预料不到的结果的证据不能排除在考虑之外,因为专利申请的时候并不总是对发明有全方位的发现。如果预料不到的技术效果可以从专利文件公开的方法隐含得出,或者与预期用途具有紧密的联系时,申请日后提交的实验中的证据应当考虑。
而我国原研药研发能力较弱,因此对于药品专利申请的补充数据要求更严格。虽然2017年我国对《专利审查指南》进行了修改,将“申请日之后补交的实施例和实验数据不予考虑”修改为“对于申请日之后补交的实验数据,审查员应当予以审查。补交实验数据所证明的技术效果应当是所属技术领域的技术人员能够从专利申请公开的内容中得到的”。在实践中,我国对“从专利申请公开的内容中得到”的判定以“直接得到”为准,而非美国的“隐含得出”。这在很多药品专利的无效、诉讼案例中都有印证。
例如,诺华重磅心衰药物的国内专利无效案:
请求人戴锦良就专利权人瑞士诺华公司(下称诺华公司)的发明专利(专利号:ZL201110029600.7)提出的无效宣告请求案,该案在审理过程中专利权人提交了组合物具有协同作用的实验数据,复审委以补交的实验数据证明了原申请中预料不到的技术效果,不能从原始申请文件中得到,因此不予接受。
又如,最高院公开宣判的武田药品专利无效案:
该案涉及专利名称为“用于治疗糖尿病的药物组合物”的发明专利,专利号为ZL96111063.5。该案的争议焦点是申请日后补充的实验数据能否被采信。该案在无效过程中,涉及一个关键性证据,即武田药品提交的反证7,反证7包括两份实验报告。第一份实验报告是证明吡格列酮与格列美脲联用具有预料不到的技术效果。该实验报告是在涉案专利的审查过程中,专利权人在答复第三次审查意见通知书时提交。第二份实验报告是证明吡格列酮和格列美脲的联用与其它格列酮类化合物和格列美脲的联用相比,具有预料不到的技术效果。该实验报告是在涉案专利相应的第EP01203170.4号欧洲专利申请的审查过程中,提交给欧洲专利局的文件。专利权人武田药品意欲通过反证7来证明发明取得了意料不到的技术效果,从而争辩发明具有创造性。然而上述理由并没有得到专利复审委和一审、二审法院的支持,反证7未被采信。
最高院的观点:从本专利审查档案来看,并无证据证明审查员是因为接受了反证7的试验数据而作出了授权决定。从欧洲同族专利审查档案来看,也无证据证明欧洲专利局接受和认可了反证7的实验数据。况且,根据专利制度的地域性原则,他国的专利审查实践对我国没有约束力。武田药品提供反证7欲证明吡格列酮与格列美脲的联合用药方案相对于单独用药方案以及其他联合用药方案均取得了意料不到的降血糖效果。但是,本专利说明书仅通过吡格列酮与伏格列波糖联用以及吡格列酮与优降糖联用的实验结果,证明胰岛素敏感性增强剂与胰岛素分泌增强剂联用相对于其中一类药物单独用药有更好的降血糖效果,并没有提及各种不同的药物联用方案之间效果的优劣。武田药品工业株式会社提交实验数据所要证明的技术效果是原始申请文件中未记载,也未证实的,不能以这样的实验数据作为评价专利创造性的依据。
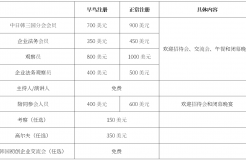
近年来医药领域的专利无效案件数量显著增多,通过统计分析以恒瑞医药、正大天晴、中信国健为代表的国内医药企业的专利无效和无效后进入行政诉讼程序的案件情况,排名前10的无效宣告请求人和无效宣告对应的专利权人如下:
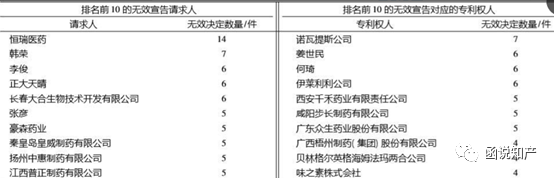
从无效成功率来看,全部无效的案子占54%;部分无效和权利要求修改后部分无效的案子占30%;维持有效和权利要求修改后维持有效的案子占16%。以上统计数据来源:“同写意”公众号,原文名称:“提出无效一个医药专利7.4个月就有决定且成功率超过50%”。
从上述案例可以看出,目前我国对于申请日后补充实验数据的规则以“直接得到”为准,较美国的“隐含得出”规则更严格。在国内,医药专利无效成功率高的很大一个原因在于补充实验数据规则偏严格,因此也造成原研药与仿制药专利大战屡遭阻击。美国依然认为2017年我国对《专利审查指南》这一适应性修改力度不够,因而成为中美贸易战中交火的议题之一。
四、《中美经贸协议》中补充实验数据规则的改变对国内药企专利布局的影响
1、对原研药企和仿制药企的影响
《中美经贸协议》中约定的补充实验数据规则,偏向美国专利法的“隐含得出”规则,更有利于原研药的专利布局。对于仿制药企而言,以后要挑战(无效)原研药专利,难度必然会增加。
2、促进国内药企开发创新药
众所周知,国内是一个仿制药大国,近两年开启的仿制药一致性评价则被业内人士称为补“历史欠账”,而通过仿制药一致性评价从而达到原研水平的药品才能入围国家带量采购品种。未来仿制药长期价格或仍将快速向下,一部分没有竞争力的仿制药必将被药企淘汰。在这一背景下,仿制药的“高毛利”时代即将结束,没有技术壁垒的普通仿制药将逐步回归制造业利润水平,而创新药将迎来快速发展期。
笔者认为,《中美经贸协议》的补充实验数据规则改变,会倒逼国内药企开发创新药,加速促进国内药企开发创新药的进程。
放眼全球医药研发领域,“国内”是决不能忽视的关键词,国内这些年在医药研发领域的成就令人瞩目,全球医药市场增速加快,新兴市场领军新的增长;国内外药审提速,国内企业迅速跟进FDA新批药物;国际多中心临床加快推开,国内制药巨头持续加码药物研发投入,国内已成为亚洲的新药研发国。在国家出台一系列鼓励药品创新的政策,加大对创新药的支持力度的情况下,创新药研发对于国内药企而言仍会是极大的发展机遇。
3、师夷之长技以制夷
国内药企应当学习国外原研药企业专利布局的成功经验,从多维度出发构建自身的专利壁垒。例如,吉利德公司有关“瑞德西韦”药物的专利布局策略,就值得国内药企借鉴和学习。
分析一下吉利德有关“瑞德西韦”药物的专利就会发现,吉利德确实已经对化合物拥有较完备的全球专利保护。吉利德公司针对瑞德西韦类似相关药物和针对病毒的治疗方法早就申请了PCT专利进行了全球专利布局,该PCT专利PCT/US2011/045102 于2011年7月22日申请,有57项同族专利申请,其中进入中国国家阶段的专利CN2011800357761“用于治疗副黏病毒科病毒感染的方法和化合物”于2015年11月25日授权,目前该专利处于有效维持状态。该专利的化合物结构使用马库什撰写方式,保护范围较宽,在治疗用途上也进行了比较上位的概括。此外,吉利德已经将瑞德西韦用于治疗冠状病毒的用途申请了专利,专利申请号为CN2016800667968,发明名称为:治疗沙粒病毒科和冠状病毒科病毒感染的方法。
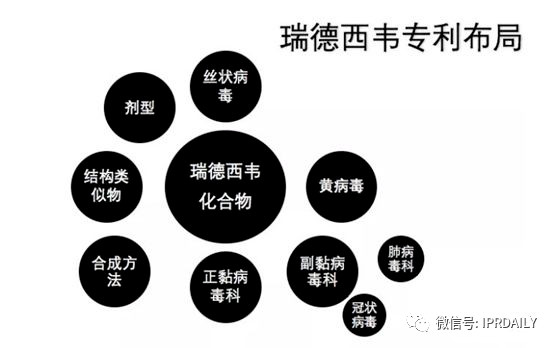
图片来源:http://www.wxshineip.cn/news/baike216.html
这让我们意识到正是由于吉利德申请的上述在先专利,对于武汉病毒研究所的专利授权带来了不小的威胁。从竞争时机的角度来看,由于吉利德重视知识产权,及时把握布局时机,压缩了竞争对手进入市场的空间。这对于国内药企在系统性的专利布局思路上有启发和借鉴意义。
4、天下武功唯快不破
《中美经贸协议》中补充实验数据规则的改变意味着补充实验数据的条件和要求放宽,给我们药企释放了一个信号:当我们有了初步的实验数据能证明物质具有一定的治疗效果,应当尽早把握专利申请时机,尽快确定申请日(优先权日),并在后续进行实验数据的完善和补充。
医药行业,创新成必然趋势,赛道拥堵加剧。资料显示,目前国内已知仍有在研PD-(L)1产品的企业有100多家,其中包括复宏汉霖、百济神州等知名创新药企。实际上不止赛道拥堵,研发也过于趋同。未来两年预计将会有10余款PD-(L)1抗体在国内获批或是申请上市,拿研发火热的PD-1来说,目前已经批了三家,后面还有30多家排队。药企想在激烈的竞争中脱颖而出,加快创新速度、及时进行专利布局无疑是最有效的策略。
5、农村包围城市——仿制药专利布局策略
对于仿制药而言,可以从外围专利布局作为突破口,采用农村包围城市的专利布局策略。具体来说,可以从制备工艺、药用辅料选择、新剂型、药物联用(组合物)等方面进行突破,寻找原研药布局中的漏网之鱼,破坏强势竞争对手的专利布局策略,通过这些专利,以换取竞争对手的交叉许可。
6、全球化专利网策略——创新药专利布局策略
对于创新药而言,特别是重磅炸弹创新药,除了化合物核心专利布局,还应从中间体、产品、组合物、制备方法、晶体等不同角度进行系列专利布局,在其他竞争对手尚未反应过来时布下一张既有深度又有广度的专利网。以阻绝竞争者的进入,对于强行侵入技术领域者,可以通过专利诉讼让竞争者付出惨痛代价。
除此之外,对创新药还应进行全球专利布局,海外国家的选择要考虑申请地是否是目标市场及潜在市场,此处市场包含产品销售地以及技术输出的目标国。《中美经贸协议》签订意味着全球化是不可阻挡的历史潮流,是全球市场经济发展、技术进步和产业价值链重塑的结果,具有客观规律的必然性。要想在全球化中受益,就要内修自身做好自己,让知识产权成为中国药企走出去的核心竞争力。
五、结语
随着全球经济一体化,知识产权在国际经济贸易中发挥着越来越重要的作用。笔者认为,《中美经贸协议》中补充实验数据规则的改变将对国内药企知识产权的规划和布局带来一定影响。未来,《专利法》和《专利审查指南》将对应做出怎样的修改,我们拭目以待。但不管何时修改,何时正式执行,《中美经贸协议》中补充实验数据规则的相关规定已经给了我们一个明确的发展方向和趋势,这是势不可挡的,不过是或早或迟而已。建议国内药企尽早做好准备,来迎接未来的挑战和机遇。
来源:IPRdaily中文网(iprdaily.cn)
作者:王函 合伙人 王则周 律师 汇业律师事务所
编辑:IPRdaily王颖 校对:IPRdaily纵横君
点击图片,查看专题详情!

「关于IPRdaily」
IPRdaily是具有全球影响力的知识产权媒体,致力于连接全球知识产权与科技创新人才。汇聚了来自于中国、美国、欧洲、俄罗斯、以色列、澳大利亚、新加坡、日本、韩国等15个国家和地区的高科技公司及成长型科技企业的管理者及科技研发或知识产权负责人,还有来自政府、律师及代理事务所、研发或服务机构的全球近100万用户(国内70余万+海外近30万),2019年全年全网页面浏览量已经突破过亿次传播。
(英文官网:iprdaily.com 中文官网:iprdaily.cn)
本文来自IPRdaily中文网(iprdaily.cn)并经IPRdaily.cn中文网编辑。转载此文章须经权利人同意,并附上出处与作者信息。文章不代表IPRdaily.cn立场,如若转载,请注明出处:“http://www.iprdaily.cn/

 共发表文章4401篇
共发表文章4401篇文章不错,犒劳下辛苦的作者吧
- 我也说两句
- 还可以输入140个字